
Wärmelehre (1)
Hier findest du alle Inhalte zur Unterrichtseinheit.
Inhalt - Wärmelehre
Teil 1:
Was ist "Wärmelehre"?
Arbeitsblatt – Temperaturen messen
Das Teilchenmodell (Kugelmodell)
Der Ölfleckversuch
Flüssigkeiten erwärmen und abkühlen
Thermometerskalen (1)
Flüssigkeiten erwärmen und abkühlen (2)
Temperatur im Teilchenmodell
Was ist Energie?
Temperatur und Energie
Thermometerskalen (2) - Die Kelvinskala
Wann siedet Wasser?
Feste Köper erwärmen und abkühlen (1)
Anwendung: Temperaturausdehnung bei Brücken
Feste Köper erwärmen und abkühlen (2)
Gase erwärmen und abkühlen
Die Anomalie von Wasser
Wärmetransport (1) - Wärmeleitung / Wärmedämmung
Wärmetransport (2) - Wärmemitführung (Konvektion)
Wärme speichern (1)
Wärme speichern (2)
Wärmetransport (3) - Wärmestrahlung
Allgemeine Hinweise zu den Themenseiten
Die hier angebotenen Themenseiten fassen die grundlegenden Inhalte, Informationen und Hefteinträge zu den Unterrichtsinhalten von verschiedenen Themenbereichen der Fächer Mathematik, Physik und dem Wahlpflichtfach MINT/Technik zusammen. Diese sind online, kostenlos und ohne Registrierung verfügbar und sollen zur besseren Selbstorganisation der Schüler beitragen.
Die im Internet bereitgestellten Materialien bieten aber auch noch zusätzliche Möglichkeiten: Sie sollen den Schülern einen Leitfaden zur Vorbereitung auf Kursarbeiten, aber auch bei Fehlstunden zur Nacharbeit der versäumten Unterrichtsinhalte dienen und weiterhin den Eltern die Möglichkeit zur Unterstützung bei den unterrichtsbegleitenden Hilfestellungen geben. Die Zusammenfassungen zu den Unterrichtsinhalten auf den Themenseiten werden dabei jeweils ergänzt durch Lernvideos, Infotexten, Aufgaben, Bildergalerien und interaktiven Tools. Diese sollen dabei helfen selbstständig eigene Ergebnisse zu überprüfen oder zusätzliche Informationen zu den Inhalten erhalten. Bei den Lernvideos handelt es sich teilweise um die YouTube-Video des YT-Kanals Mathe-Physik-Technik. Weiterhin sind bei den einzelnen Folien zusätzliche Videovorschläge von anderen YouTube-Kanälen zugeordnet. Der jeweilige Link leitet dann ggf. direkt auf die YouTube-Video-Seite weiter.
Bei den klassischen physikalischen Themenbereichen sind die jeweiligen Folien für den digitalen Unterricht weitestgehend angepasst und optimiert worden. Insbesondere durch die Corona-Krise rückt der digitale und eigenverantwortliche Unterricht immer mehr in den Fokus. Zu den einzelnen Folien sind deshalb jeweils passende Videos zu den Inhalten zugeordnet und zu vielen Folien auch passende Aufgaben eingearbeitet worden. Dadurch sind die Themenbereiche in Teilabschnitten strukturiert und für die Arbeit mit Wochenplänen optimiert worden. Sie ermöglichen den Schülern so die selbstständige Arbeit daheim und geben jedem Schüler die Möglichkeit die Lernziele auch unter den gegebenen Umständen bestmöglich zu erreichen. Dabei können Schüler dann sogar die positiven Seiten des digitalen Unterrichts (Eigenes Lerntempo festlegen, optimale Anpassung von Lernzeit und Zeitpunkt an den eigenen Biorhythmus zum effizienten Lernen, etc.) für sich besonders gut nutzen.
Siehe hierzu auch: → Konzept - mathe-physik-technik.de
Skript → Publikationen
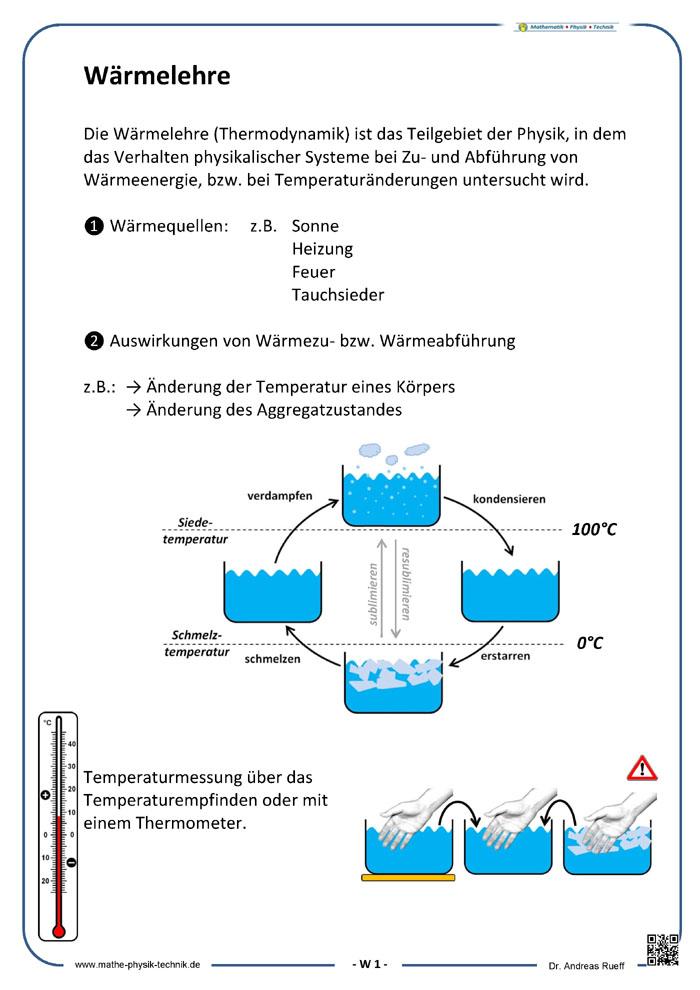

Infotext - [01] Wärmelehre
Die Wärmelehre oder Thermodynamik (von altgriechisch thermós, deutsch ‚warm‘, sowie dýnamis, deutsch ‚Kraft‘) ist eine natur- und ingenieurwissenschaftliche Disziplin. Sie hat ihren Ursprung im Studium der Dampfmaschinen und ging der Frage nach, wie man Wärme in mechanische Arbeit umwandeln kann. Dazu beschreibt sie physikalische Systeme und deren Zustandsübergänge (→Aggregatszustände). Als Ingenieurwissenschaft hat sie für die verschiedenen Möglichkeiten der Energieumwandlung Bedeutung und für das Verhalten von Stoffen. Als Begründer gilt der französische Physiker Sadi Carnot (1796-1832), der 1824 seine wegweisende Arbeit schrieb.
Die Wärmelehre befasst sich einerseits mit verschiedenen Prozessen, ohne auf die Besonderheiten der daran beteiligten Stoffe einzugehen. Andererseits macht sie Aussagen über Stoffe wie die
verschiedenen Aggregatzustände und ihren Wechsel (schmelzen, sieden, verdampfen …) oder chemische Reaktionen, die sehr stark von den jeweiligen Stoffen abhängen.
Aggregatzustände sind fundamentale Erscheinungsformen von Materie. Die Aggregatzustände fest, flüssig und gasförmig lassen sich leicht anhand ihrer unterschiedlichen
mechanischen Eigenschaften identifizieren. Die Überführung eines Stoffes in einen anderen Aggregatzustand erfolgt durch eine Zustandsänderung, etwa durch eine Änderung der Temperatur oder des
Volumens.
Es gibt drei Aggregatzustände:
- fest: Ein Stoff behält Form als auch Volumen bei.
- flüssig: Hier wird das Volumen beibehalten, aber die Form ist unbeständig.
- gasförmig: Die Volumenbeständigkeit entfällt, ein Gas füllt den zur Verfügung stehenden Raum vollständig aus.
Übergänge zwischen den verschiedenen Aggregatzuständen: (Alle Übergänge können am Beispiel Wasser im Alltag beobachtet werden.)
- Schmelzen: Bei Temperaturen oberhalb der Schmelztemperatur wird Schnee oder Eis im Frühjahr flüssig.
- Erstarren: Kühlt Wasser unter den Gefrierpunkt ab, bilden sich Eiskristalle, die mit der Zeit immer größer werden, bis die Oberfläche mit einer Eisschicht überzogen ist.
- Verdampfen: Wird Wasser im Kochtopf über seine Siedetemperatur erhitzt, so wird das Wasser gasförmig. Die aufsteigenden Blasen sind der Wasserdampf. (Verdunstung, der Übergang von flüssig in gasförmig ohne Erreichen der Siedetemperatur, ist bei Wasser auf einer Straße zu beobachten.)
- Kondensieren: Beim Duschen „beschlägt“ der Spiegel im Badezimmer. Wasserdampf ist dabei, durch die niedrige Temperatur des Spiegels, in den flüssigen Zustand überführt worden.

-----------------------------------
Hinweis: Die Quellenangaben zu diesem Text sind am Ende dieser Internetseite zu finden.
Videos:
1) → FWU - Teilchenmodell und Aggregatzustände
2) → Aggregatzustände einfach erklärt (Mit Infos für "Experten")
3) → Aggregatzustände I fest I flüssig I gasförmig
Anmerkung: Die Links in diesem Ordner verweisen auf externe YouTube-Videos anderer YouTube-Kanäle. Gelegentlich werden Videos dort auch wieder entfernt. Entsprechende Hinweise zur Aktualisierung dieser Seite werden gerne per → Mail oder über das → Kontaktformular entgegengenommen. - Vielen Dank schon vorab für den Hinweis!
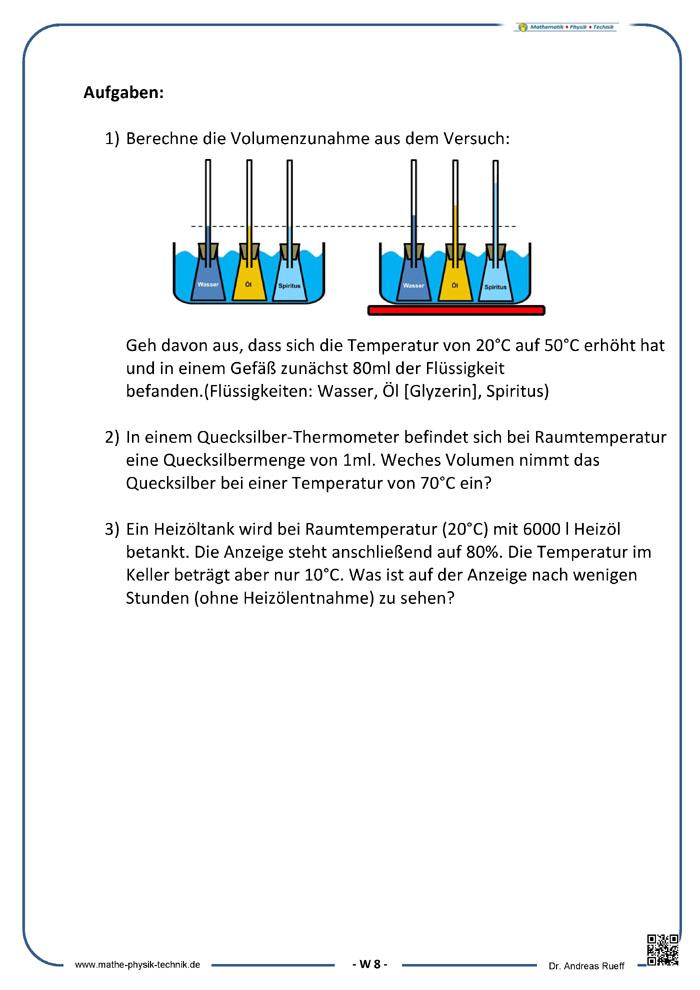
Aufgaben:
Anmerkung: Die Online-Übung in diesem Ordner ist evtl. eine externe Übung. Angaben zum Ersteller sind
teilweise (manchmal) auch in der Übung angegeben. Links in diesem Ordner verweisen evtl. auf externe Inhalte.
Gelegentlich werden Übungen vom Ersteller auch wieder entfernt. Entsprechende Hinweise zur Aktualisierung dieser Seite oder auch Hinweise zu Inhalten werden gerne per
→ Mail
oder über das → Kontaktformular entgegengenommen. - Vielen Dank
schon vorab für den Hinweis!
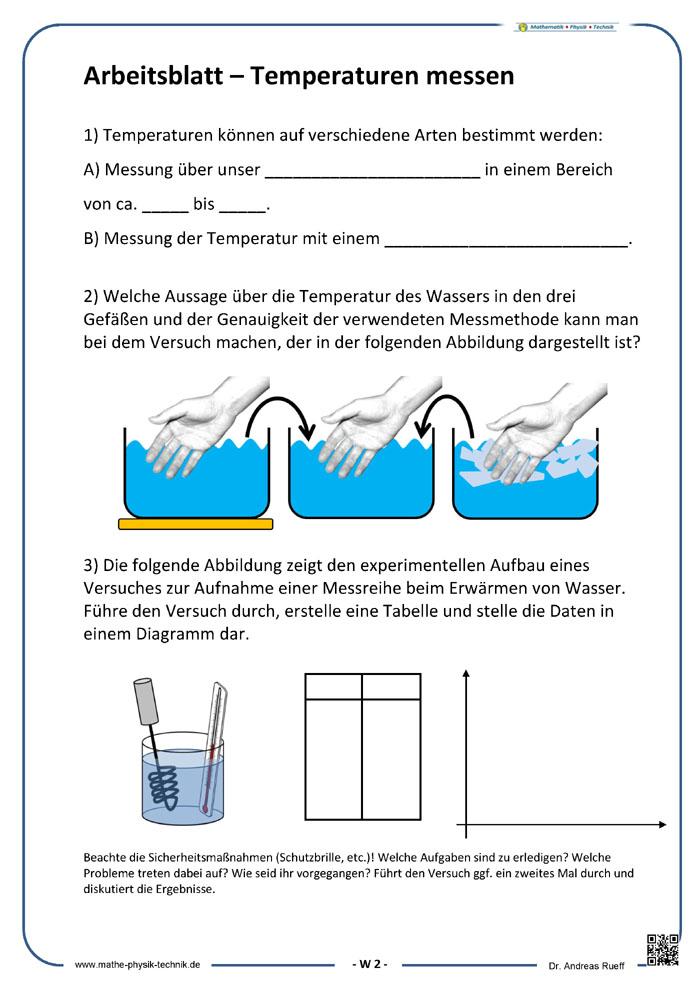
Temperatursinn und Thermometer
Temperaturempfinden
Als Temperatursinn (auch Thermorezeption) wird die Fähigkeit von Lebewesen bezeichnet Temperaturen zu fühlen und zu ertasten. Nervenzell-Enden (Rezeptorzellen) in der Haut oder in den
Schleimhäuten versetzen uns in die Lage Temperaturen wahrzunehmen. Sie erzeugen Nervenimpulse die sich in Abhängigkeit von der Temperatur verändern. Diese Impulse werden über die Nervenfasern
bis zum Gehirn weitergeleitet. Thermorezeptoren bilden die Grundlage der Temperaturwahrnehmung. Damit können wir Temperaturen die etwa zwischen 15°C und 45°C liegen recht gut zuordnen und
voneinander unterscheiden. Im Bereich von 37°C ist der Temperatursinn sehr empfindlich. Deshalb lässt sich bei Menschen mit der Hand sogar ertasten, ob beispielsweise ein Kind Fieber hat. Der
Temperatursinn lässt sich aber auch leicht täuschen. Wir bewerten einen Sinneseindruck nämlich immer dadurch, dass wir mit der zuvor wahrgenommenen Temperatur vergleichen. So kann eine
bestimmte Temperatur von zwei Personen unterschiedlich (als warm oder kalt) bewertet werden. Nach einer kalten Dusche erscheint uns beispielsweise das Wasser im Becken eines Schwimmbades als
warm, ohne die kalte Dusche kommt es uns dagegen kälter vor. Eine wirklich objektive Bewertung der Temperatur ist als durch den Temperatursinn nicht möglich
Außerdem wirken sie an der Thermoregulation im Körper mit. Bei einigen Lebewesen sind Thermorezeptoren zu speziellen Sinnesorganen gebündelt, die der Orientierung (Navigation) oder der
Beutefindung dienen. Zu den Pionieren der wissenschaftlichen Erforschung des Temperatursinns gehören die Physiologen Ernst Heinrich Weber und Max von Frey. Für die Entdeckung der
Thermorezeptoren erhielten David Julius und Ardem Patapoutian 2021 den Nobelpreis für Medizin.
Thermometer
 Ein Thermometer (altgriechisch θερμός thermós, deutsch ‚warm‘ und altgriechisch μέτρον métron, deutsch ‚Maß, Maßstab‘) ist ein
Messgerät zur Bestimmung der Temperatur. Die Temperatur wird damit durch einen Zahlenwert beschrieben und ist unabhängig von unserem Temperatursinn, also eine objektive Bewertung der
Eigenschaft eines Körpers.
Ein Thermometer (altgriechisch θερμός thermós, deutsch ‚warm‘ und altgriechisch μέτρον métron, deutsch ‚Maß, Maßstab‘) ist ein
Messgerät zur Bestimmung der Temperatur. Die Temperatur wird damit durch einen Zahlenwert beschrieben und ist unabhängig von unserem Temperatursinn, also eine objektive Bewertung der
Eigenschaft eines Körpers.
Thermometer können auf verschiedene Art funktionieren und sind deshalb in unterschiedlichen Bereichen einsetzbar. Thermometer bestehen aus einem Temperatur-Sensor (in dem der Messeffekt
auftritt) und einer Anzeige (z. B. anhand einer Skala).
-----------------------------------
Hinweis: Die Quellenangaben zu diesem Text sind am Ende dieser Internetseite zu finden.
Videos:
1) → Wärmeempfindung | alpha Lernen erklärt Physik
2) → Temperaturmessung | alpha Lernen erklärt Physik
3) → Heiss-Kalt Wasserexperiment!
Anmerkung: Die Links in diesem Ordner verweisen auf externe YouTube-Videos anderer YouTube-Kanäle. Gelegentlich werden Videos dort auch wieder entfernt. Entsprechende Hinweise zur Aktualisierung dieser Seite werden gerne per → Mail oder über das → Kontaktformular entgegengenommen. - Vielen Dank schon vorab für den Hinweis!
Aufgaben:

Seifenblase einfrieren [1:51]
Der Winter 2018 machte es möglich!
Eine einfache Seifenblase wird am 27. Feb. 2018 bei -10°C in Kaiserslautern eingefroren.

Infotext - Das Teilchenmodell
Das Teilchenmodell ist eine der einfachsten Modellvorstellungen zum Aufbau der Materie. Es beruht auf der Grundannahme, dass ausgedehnte Körper aus vielen einzelnen Teilchen bestehen, die erst durch ihr Zusammenwirken die Eigenschaften entstehen lassen, die sich in den makroskopischen Zuständen und Vorgängen zeigen (Begriffserklärung: Makroskopisch → mit bloßem Auge sichtbar, Mikroskopisch → nur mit Gerät zur Vergrößerung, z. B. Lupe oder Mikroskop, sichtbar). Als (nahezu) unveränderliche Teilchen dieser Art wurden die Atome identifiziert. Ihre Anzahl übertrifft schon bei kleinen makroskopischen Körpern leicht die Größenordnung einer 23-stelligen Zahl.
Erklärungen mit Hilfe des Teilchenmodells
Das Teilchenmodell geht davon aus, dass die Teilchen eines reinen Stoffs alle identisch zueinander sind. Sie unterscheiden sich aber von den Teilchen anderer Stoffe, zum Beispiel in ihrer Größe, Form oder Masse. Über den inneren Aufbau der Teilchen wird keine Aussage gemacht.
Im einfachsten Ansatz werden die Teilchen als harte Kugeln dargestellt. Dieses Teilchenmodell ist schon geeignet für die Beschreibung der Körper im gasförmigen Zustand. In der nächsten Stufe des Modells werden Teilchen angenommen, die sich nach festen Regeln mit anderen Teilchen stabil verbinden können. Schließlich wird das Teilchenmodell dadurch erweitert, dass die Teilchen bei starker Annäherung abstoßende und bei mittlerer Entfernung anziehende Kräfte aufeinander ausüben können. Unter anderem lassen sich folgende Beobachtungen im Rahmen dieses Teilchenmodells erklären:
- Mechanische Festigkeit von festen Körpern
- Leichte Verformbarkeit von Flüssigkeiten und Gasen.
- Die Aggregatzustände (fest, flüssig, Gasförmig) und deren Umwandlung ineinander. Sie werden bestimmt durch die Anziehung der Teilchen zueinander.
- Die Komprimierbarkeit der Gase durch große Abstände zwischen den Teilchen.
- Bei Flüssigkeiten und Feststoffen kann das Volumen fast gar nicht verringert werden, weil die Teilchen bereits nahe beieinander sind.
„Die wichtigste Erkenntnis der Physik“
Um die Bedeutung des Teilchenmodells gebührend zu würdigen, stellte der große Physiker Richard Feynman ( 1918 – 1988, US-amerikanischer Physiker und
Nobelpreisträger für Physik 1965) die Frage, welche Erkenntnis der Physik es wert sei, der Nachwelt überliefert zu werden, wenn man nur Gelegenheit zu einem einzigen Satz hätte. Seine
Antwort:
„Alle Dinge bestehen aus Atomen - kleinen Teilchen, die sich ewig bewegen, einander anziehen, wenn sie etwas Abstand haben, jedoch abstoßen, wenn sie gegeneinandergedrückt werden.“

-----------------------------------
Hinweis: Die Quellenangaben zu diesem Text sind am Ende dieser Internetseite zu finden.
Videos:
1) → Teilchenmodell, erster Lehrsatz | alpha Lernen erklärt Physik
2) → FWU - Teilchenmodell und Aggregatzustände
3) → Teilchenmodell I Atome I Moleküle
4) → Das Teilchenmodell einfach erklärt ("Expertenvideo" mit Zusatzinformationen)
Anmerkung: Die Links in diesem Ordner verweisen auf externe YouTube-Videos anderer YouTube-Kanäle. Gelegentlich werden Videos dort auch wieder entfernt. Entsprechende Hinweise zur Aktualisierung dieser Seite werden gerne per → Mail oder über das → Kontaktformular entgegengenommen. - Vielen Dank schon vorab für den Hinweis!
Aufgaben:
Anmerkung: Die Online-Übung in diesem Ordner ist evtl. eine externe Übung. Angaben zum Ersteller sind
teilweise (manchmal) auch in der Übung angegeben. Links in diesem Ordner verweisen evtl. auf externe Inhalte.
Gelegentlich werden Übungen vom Ersteller auch wieder entfernt. Entsprechende Hinweise zur Aktualisierung dieser Seite oder auch Hinweise zu Inhalten werden gerne per
→ Mail
oder über das → Kontaktformular entgegengenommen. - Vielen Dank
schon vorab für den Hinweis!
-----------------------------------
Hinweis: Die Quellenangaben zu diesem Text sind am Ende dieser Internetseite zu finden.
Anmerkung: Die Online-Übung in diesem Ordner ist eine externe Übung. Angaben zum Ersteller sind teilweise
(manchmal) auch in der Übung angegeben. Links in diesem Ordner verweisen evtl. auf externe Inhalte.
Gelegentlich werden Übungen vom Ersteller auch wieder entfernt. Entsprechende Hinweise zur Aktualisierung dieser Seite oder auch Hinweise zu Inhalten werden gerne per
→ Mail
oder über das → Kontaktformular entgegengenommen. - Vielen Dank
schon vorab für den Hinweis!
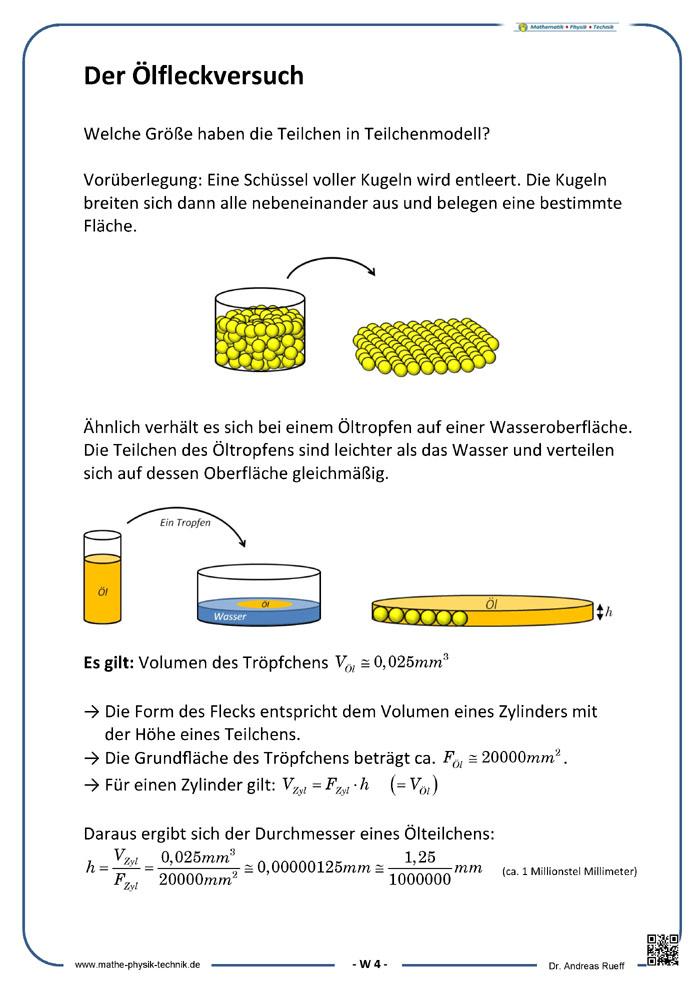
Infotext - Der Ölfleckversuch
Der Ölfleckversuch ist ein Versuch aus der Chemie und Physik, der es mit einfachen Mitteln möglich macht, die Größe eines Moleküls (Atoms) näherungsweise zu bestimmen.
Einen solchen Versuch führte Benjamin Franklin bereits 1774 durch (Franklin war Verleger, Schriftsteller, Naturwissenschaftler, Erfinder und als Staatsmann einer der Gründerväter der Vereinigten Staaten von Amerika). Ein Teelöffel Öl breitete sich dabei auf einem glatten See auf einer bestimmten Fläche aus. Aus dem Volumen des Öltropfens und der Fläche ließe sich damals schon die Dicke des Ölfilms bestimmen (rund 10−10 m), einen Schluss, den Franklin allerdings nicht vollzog. Franklin war damals noch nicht an Moleküldimensionen interessiert, sondern wie andere Wissenschaftler seiner Zeit an Methoden mit Öl die Wasserwogen zu glätten. Der Beitrag von Franklin geriet bald darauf in Vergessenheit, in Großbritannien auch wegen seiner Beteiligung am Unabhängigkeitskrieg der USA. Interesse daran erwachte erst wieder Ende des 19. Jahrhunderts, als Lord Rayleigh (der Franklins Experiment kannte) ihn in öffentlichen Vorlesungen in der Royal Institution 1890 wiederholte und daraus Moleküldimensionen abschätzte.
Versuch
Auf eine mit Wasser gefüllte Schale wird eine feine Schicht Bärlappsporen – oder ein ähnliches Pulver – gepudert. Diese dienen dazu, die Wasseroberfläche besser sichtbar zu machen. Anschließend wird ein Tropfen eines Gemischs aus Öl und Benzin mit bekannter Konzentration (1:1000) und zuvor bestimmtem Volumen in die Mitte der Schale gegeben. Das Benzin dient einer gleichmäßigen schnellen Verteilung des Öls auf dem Wasser und der Verdünnung des Öls. Das Benzin verdunstet dann und ein Fleck aus reinem Öl verbleibt auf der Wasseroberfläche. Dieser verdrängt die Bärlappsporen kreisförmig an den Rand der Schale, weshalb er deutlich sichtbar ist und mit einem Lineal vermessen werden kann. Von grundlegender Bedeutung ist die Annahme, dass es sich bei dem Ölfleck um eine monomolekulare Schicht handelt, das heißt, dass sich nicht mehrere Moleküle übereinander befinden.
Auswertung
Einen möglichst runden Fleck kann man nun als Zylinder betrachten, wobei der Durchmesser eines Moleküls der Höhe des Zylinders entspricht. Über das Volumen des Tropfens und die Konzentration des Benzin-Öl-Gemischs kann man nun das Volumen des Öls ausrechnen. Das ist mit dem Volumen des Zylinders identisch. Mit dem abgemessenen Radius kann man nun die Höhe des Zylinders und damit die ungefähre Größe eines Ölmoleküls berechnen.

-----------------------------------
Hinweis: Die Quellenangaben zu diesem Text sind am Ende dieser Internetseite zu finden.

Hintergrundinformationen - Geometrie: Der Zylinder [4:21]
Die Volumenformel
Die Volumenformel eines Zylinders wird anschaulich hergeleitet. Anschließend werden die Ergebnisse zusammengefasst und ein Beispiel vorgerechnet.
Videos:
1) → Ölfleckversuch - einfach und anschaulich erklärt
Anmerkung: Die Links in diesem Ordner verweisen auf externe YouTube-Videos anderer YouTube-Kanäle. Gelegentlich werden Videos dort auch wieder entfernt. Entsprechende Hinweise zur Aktualisierung dieser Seite werden gerne per → Mail oder über das → Kontaktformular entgegengenommen. - Vielen Dank schon vorab für den Hinweis!
Aufgaben:
- Was genau möchte man mit dem Ölfleckversuch eigentlich herausfinden?
- Heute gibt es für viele Dinge doch sehr genaue Messmethoden. Warum ist der Ölfleckversuch trotzdem so interessant für uns, gerade in der Schule?
- Warum benötigt man eigentlich das Wasser in diesem Versuch?
- Beim Versuch werden Bärlappsporen auf die Wasseroberfläche gegeben. Was ist der Grund dafür?
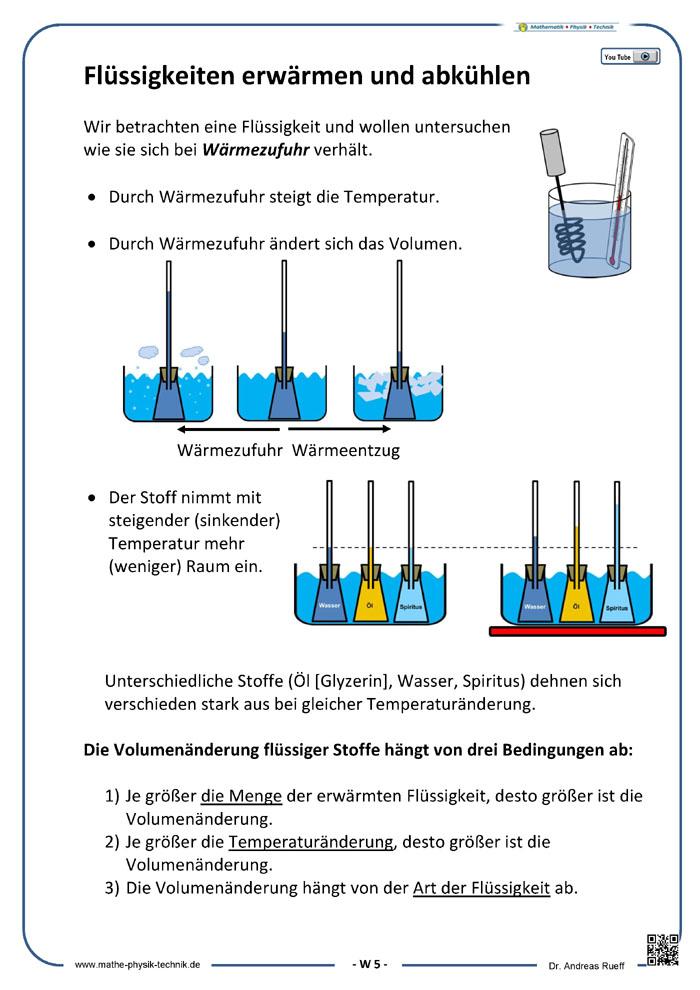
Infotext - Flüssigkeiten erwärmen und abkühlen

-----------------------------------
Hinweis: Die Quellenangaben zu diesem Text sind am Ende dieser Internetseite zu finden.

Wärmelehre: [8:46]
Wärmeausdehnung von Flüssigkeiten
Gezeigt wird zunächst die Ausdehnung von Wasser bei Temperaturerhöhung. Weiterhin werden anschließend drei verschiedene Flüssigkeiten erwärmt und die Ergebnisse präsentiert. Die Anwendung der Ergebnisse bei der Festlegung der Celsiusskala wird als Anwendung erläutert.
Aufgaben:
- Getränkeflaschen sind nie völlig bis zum Rand befüllt. Welchen Grund könnte das haben?
- Der Benzintank eines Fahrzeugs sollte nie ganz aufgefüllt werden, das gilt besonders im Sommer. Warum muss man hier besonders vorsichtig sein?
- Wenn du Wasser in ein Trinkglas füllst und es dann erwärmst (z.B. von 20°C auf 50°C), dann ist „eigentlich“ kein Anstieg des Wasserstands im Glas zu beobachten. Beim Versuch konntest du aber die Volumenänderung deutlich erkennen. Was ist der Grund dafür?

Infotext - Thermometerskalen (1)
Die Celsius-Temperaturskala
Anders Celsius (1701 - 1744) war ein schwedischer Astronom, Mathematiker und Physiker. Er wurde 1701 in Uppsala geboren. Er studierte an der Universität Uppsala und wurde dort 1730 Professor.
1736 nahm Celsius an einer Expedition zur Vermessung der Form der Erde teil. 1741 stellte er die erste schwedische Sternwarte in Uppsala fertig. Er war außerdem auch Autor
populärwissenschaftlicher Literatur. Celsius war der Erste, der die Helligkeit von Sternen messtechnisch untersuchte; auch fand er heraus, dass Polarlichter das Magnetfeld der Erde
stören.
Anders Celsius definierte 1742 die nach ihm benannte Temperatureinteilung Grad Celsius. Im Gegensatz zur heute verwendeten Celsius-Skala legte er den
Siedepunkt von Wasser mit 0° und den Gefrierpunkt mit 100° fest. Durch Carl von Linné wurden die Fixpunkte der Skala vertauscht; heutzutage wird sie ausschließlich
in letzterer Form verwendet. Das Revolutionäre war, dass Celsius vorgeschlagen hatte, sie als universelle Skala zu benutzen, um Temperaturen in der ganzen Welt zu
vergleichen: Im Gegensatz zu anderen Forschern notierte er bei der genauen Bestimmung der Fixpunkte auch den herrschenden Luftdruck und legte so genaue Messbedingungen
fest.
1948, ca. 200 Jahre nach der Einführung der Skala, wurde zu Ehren Celsius’ durch die 9. internationale Generalkonferenz für Maß und Gewicht offiziell in die Temperatureinheit Grad
Celsius (°C) festgelegt. Das Originalthermometer kann heute im Museum der Universität Uppsala, dem Gustavianum, besichtigt werden. Es besteht, genau wie ein heutiges
Thermometer, aus einem auf ein Holzbrett mit Skala montierten Quecksilberreservoir mit angesetzter Kapillare (Glasröhrchen).
Die Fahrenheit-Temperaturskala
Grad Fahrenheit (°F) ist eine Maßeinheit der Temperatur. Sie wurde nach dem deutschen Physiker Daniel Gabriel Fahrenheit (1686–1736) benannt. Fahrenheit entwickelte seine Temperaturskala nach einem Besuch bei dem dänischen Astronomen Ole Rømer in Kopenhagen. Rømer war der Erste, der ein Thermometer entwickelte, das mit Hilfe zweier Fixpunkte kalibriert (kalibrieren = überprüfen der Messtoleranzen zu einem bekannt richtigen Standard) wurde. Fahrenheit verwendete demgegenüber als Nullpunkt seiner Skala die tiefste Temperatur, die er mit einer Mischung aus Eis, Wasser und Salz (Kältemischung) erzeugen konnte: −17,8 °C, welche 0 °F entsprechen. Dadurch wollte er in seiner Skala negative Werte vermeiden. Als zweiten Fixpunkt legte Fahrenheit die Körpertemperatur eines „gesunden Menschen“ fest.

-----------------------------------
Hinweis: Die Quellenangaben zu diesem Text sind am Ende dieser Internetseite zu finden.
Videos:
1) → Wärmeausdehnung von Flüssigkeiten
2) → Volumenausdehnung von Alkohol und Wasser
3) → Wärmeausdehnung von Flüssigkeiten - Beispiel Wasser
4) → Temperaturmessung | alpha Lernen erklärt Physik
5) → Thermometer: Wie funktioniert das? – Physik | Duden Learnattack
Anmerkung: Die Links in diesem Ordner verweisen auf externe YouTube-Videos anderer YouTube-Kanäle. Gelegentlich werden Videos dort auch wieder entfernt. Entsprechende Hinweise zur Aktualisierung dieser Seite werden gerne per → Mail oder über das → Kontaktformular entgegengenommen. - Vielen Dank schon vorab für den Hinweis!
Aufgaben:
-
Beschreibe den Aufbau und die Funktionsweise eines Flüssigkeitsthermometers.Beschreibe die Vorgehensweise zum Bau eines Flüssigkeitsthermometers. Mit dem Thermometer sollen Temperaturen im Bereich von -10°C bis 100°C gemessen werden.
-
Die Temperaturangaben in Deutschland und den USA unterscheiden sich deutlich. Was ist der Grund?
-
Schau dir die "Bildergalerie - Thermometer" an. In Abbildung 1 sind verschiedene Thermometer dargestellt. Beschreibe sie, nenne drei Unterschiede und drei Gemeinsamkeiten. Die Steighöhe der Flüssigkeiten in den Thermometern ist verschieden, sie zeigen aber trotzdem die gleiche Temperatur. Wie kommt das?
-
In Abbildung 2 siehst du auch ein Thermometer. Das ist ein „Galileo-Thermometer“. Auch das ist ein Flüssigkeitsthermometer. Wie funktioniert es?
Anmerkung: Die Online-Übung in diesem Ordner ist eine externe Übung. Angaben zum Ersteller sind teilweise
(manchmal) auch in der Übung angegeben. Links in diesem Ordner verweisen evtl. auf externe Inhalte.
Gelegentlich werden Übungen vom Ersteller auch wieder entfernt. Entsprechende Hinweise zur Aktualisierung dieser Seite oder auch Hinweise zu Inhalten werden gerne per
→ Mail
oder über das → Kontaktformular entgegengenommen. - Vielen Dank
schon vorab für den Hinweis!
Diese App wurde erstellt von Werner Glanz bei LearningApps.org
Anmerkung: Die Online-Übung in diesem Ordner ist eine externe Übung. Angaben zum Ersteller sind teilweise (manchmal) auch in der Übung angegeben. Links in diesem Ordner
verweisen evtl. auf externe Inhalte.
Gelegentlich werden Übungen vom Ersteller auch wieder entfernt. Entsprechende Hinweise zur Aktualisierung dieser Seite oder auch Hinweise zu Inhalten werden gerne per
→ Mail
oder über das → Kontaktformular entgegengenommen. - Vielen Dank
schon vorab für den Hinweis!


Diese App wurde erstellt von Dr. A. Rueff bei LearningApps.org
Anmerkung: Die Online-Übung in diesem Ordner ist eine externe Übung. Angaben zum Ersteller sind teilweise (manchmal) auch in der Übung angegeben. Links in diesem Ordner
verweisen evtl. auf externe Inhalte.
Gelegentlich werden Übungen vom Ersteller auch wieder entfernt. Entsprechende Hinweise zur Aktualisierung dieser Seite oder auch Hinweise zu Inhalten werden gerne per
→ Mail
oder über das → Kontaktformular entgegengenommen. - Vielen Dank
schon vorab für den Hinweis!
Diese App wurde erstellt von Dr. A. Rueff bei LearningApps.org
Anmerkung: Die Online-Übung in diesem Ordner ist eine externe Übung. Angaben zum Ersteller sind teilweise (manchmal) auch in der Übung angegeben. Links in diesem Ordner
verweisen evtl. auf externe Inhalte.
Gelegentlich werden Übungen vom Ersteller auch wieder entfernt. Entsprechende Hinweise zur Aktualisierung dieser Seite oder auch Hinweise zu Inhalten werden gerne per
→ Mail
oder über das → Kontaktformular entgegengenommen. - Vielen Dank
schon vorab für den Hinweis!
Bildergalerie 1: Thermometer

Infotext - Temperatur im Teilchenmodell (brownsche Bewegung)
Die brownsche Bewegung ist die vom schottischen Botaniker Robert Brown im Jahr 1827 unter dem Mikroskop entdeckte unregelmäßige und ruckartige Wärmebewegung kleiner Teilchen in Flüssigkeiten und Gasen. Robert Brown (1773 - 1858) war schottischer Arzt und ein bedeutender Botaniker.
Bei der Beobachtung von Blütenpollen in einem Wassertropfen stellte Brown 1827 fest, dass die Beobachtung der Pollen durch ständige unregelmäßige und ruckartige Bewegungen gestört wurde. Zunächst wartete Brown eine Weile und vermutete, dass sich die Bewegung mit der Zeit verringern müsste und irgendwann aufhören sollte. Aber auch nach einer längeren Wartezeit hörte die beobachtete Bewegung nicht auf. Ursprünglich nahm Brown an, dass die beobachtete Bewegung ein Hinweis auf eine den Pollen innewohnende Lebenskraft sei, wie sie lange Zeit von Wissenschaftlern als existent vermutet wurde. Jedoch konnte er die gleiche Bewegung dann auch an sicher unbelebten Staubkörnern oder fein zerstäubter Asche in Wasser beobachten. Nach Browns Veröffentlichung erbrachten detaillierte Experimente zunehmend die Gewissheit, dass die brownsche Bewegung eine allgemeine und grundsätzliche Erscheinung ist. Sie wird also durch die Bewegung unsichtbarer und sehr kleiner Flüssigkeitsteilchen hervorgerufen. Diese Flüssigkeitsteilchen sind dabei selbst sehr viel kleiner als die sichtbaren Pollen oder Staubteilchen. Die unsichtbaren Flüssigkeitsteilchen stoßen durch ihre eigene Bewegung immer wieder gegen die viel größeren Staubteilchen und führen so zu deren sichtbarer Bewegung. Dieser Prozess wirkt dabei dann ganz allgemein umso stärker, je höher die Temperatur eines Körpers ist. Damit ergab sich aus der brownschen Bewegung der erste Nachweis der im Teilchenmodell angenommenen allgemeinen Wärmebewegung aller Teilchen.
Auch Albert Einstein beschäftigte sich mit diesem Thema. Im Jahr 1905 wurde von ihm eine Erklärung gegeben: Die im Mikroskop sichtbare Verschiebung der Teilchen wird demnach dadurch bewirkt, dass die Moleküle aufgrund ihrer ungeordneten Wärmebewegung ständig und aus allen Richtungen in großer Zahl gegen die Teilchen stoßen und dabei rein zufällig mal die eine Richtung, mal die andere Richtung stärker zum Tragen kommt. Die erfolgreiche Erklärung der brownschen Bewegung gilt als Meilenstein auf dem Weg zum wissenschaftlichen Nachweis der Existenz der Moleküle und Atome.

-----------------------------------
Hinweis: Die Quellenangaben zu diesem Text sind am Ende dieser Internetseite zu finden.
Videos:
1) → Brownsche Molekularbewegung [1:50]
2) → Was ist die Brownsche Bewegung? [2:58]
3) → Brown'sche Molekularbewegung: Milch auf warmen Wasser (Versuch) [1:05]
4) → Teilchenmodell, erster Lehrsatz | alpha Lernen erklärt Physik [2:44]
Anmerkung: Die Links in diesem Ordner verweisen auf externe YouTube-Videos anderer YouTube-Kanäle. Gelegentlich werden Videos dort auch wieder entfernt. Entsprechende Hinweise zur Aktualisierung dieser Seite werden gerne per → Mail oder über das → Kontaktformular entgegengenommen. - Vielen Dank schon vorab für den Hinweis!
Aufgaben:

- Stell dir vor, dass im Herbst ein Blatt von einem Baum fällt und auf einem Ameisenhaufen landet.
a) Welche Beobachtung wirst du dann aus einer weiteren Entfernung (ca. 10 m) machen?
b) Welche Beobachtung kannst du aus einer kurzen Entfernung (ca. 50 cm) machen?
c) Was hat das mit der Brownschen Bewegung zu tun? - Wäre die Beobachtung der Brownschen Bewegung auch sichtbar, wenn man die Pollen in einem Eiswürfel einfriert und sie dort unter dem Mikroskop beobachtet?
- Kann man die Brownsche Bewegung auch in Gasen beobachten? Begründe deine Antwort mit einem Beispiel und erläutere deine Überlegungen.
Infotext - [09/10] Was ist Energie?

Die Energie (oder auch Energiemenge) ist eine fundamentale physikalische Größe, die in allen Teilgebieten der Physik sowie in der Technik, Chemie, Biologie und der Wirtschaft eine zentrale Rolle spielt.
 Energie wird in der Einheit Joule
angegeben. James Prescott Joule (1818 - 1889) war ein britischer Brauer, der als Physiker zu größten Ehren kam. Als Spross einer Brauerfamilie war er selbst Besitzer einer
Bierbrauerei und forschte, ausgehend von technischen Fragen des Maschinenbaus und des Brauereiwesens, zu naturwissenschaftlichen Fragen. Er leistete einen wesentlichen Beitrag zur
Weiterentwicklung der Wissenschaften. Die Einheit der Energie wurde deshalb ihm zu Ehren „Joule“ genannt.
Energie wird in der Einheit Joule
angegeben. James Prescott Joule (1818 - 1889) war ein britischer Brauer, der als Physiker zu größten Ehren kam. Als Spross einer Brauerfamilie war er selbst Besitzer einer
Bierbrauerei und forschte, ausgehend von technischen Fragen des Maschinenbaus und des Brauereiwesens, zu naturwissenschaftlichen Fragen. Er leistete einen wesentlichen Beitrag zur
Weiterentwicklung der Wissenschaften. Die Einheit der Energie wurde deshalb ihm zu Ehren „Joule“ genannt.
1841 veröffentlichte der deutsche Arzt Julius Robert Mayer die Idee, dass Energie weder erschaffen noch vernichtet, sondern nur umgewandelt werden kann. In einem gegenüber der Umgebung abgeschlossenen System ändert sich die Gesamtenergie also demnach nicht. Das ist die Aussage des Energieerhaltungssatzes. Eine Dampfmaschine wandelt beispielsweise Wärmeenergie in mechanische Energie um. Die Wärmeenergie, die während des Betriebs einer Dampfmaschine verloren gegangen ist, entspräche genau der mechanischen Arbeit, die die Maschine leistet.
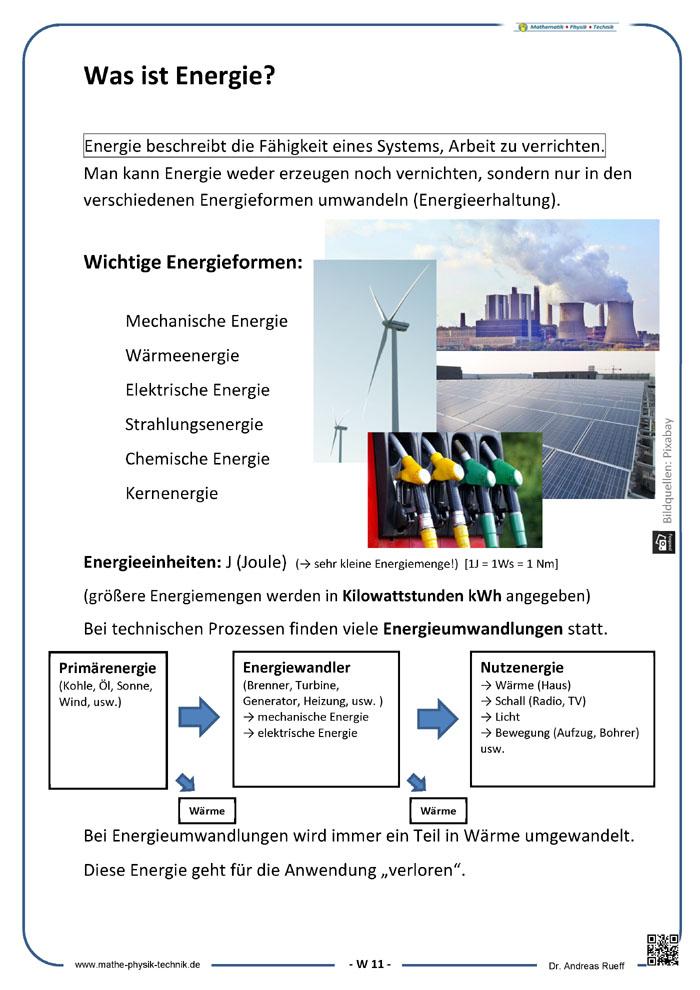
Energieformen
Energie gibt es in verschiedenen Energieformen, die ineinander umgewandelt werden können. von Energieformen sind Lageenergie (potentielle Energie), Bewegungsenergie (kinetische Energie), elektrische, chemische und Wärmeenergie (thermische Energie). Beispiele für solche Umwandlungen von Energie sind, dass ein Mensch ein Paket hochhebt (Beim Herunterfallen wird die potentielle Energie dann wieder frei) oder eine Batterie aufgeladen wird.
Technische Nutzung der Energie
Eine Erzeugung von Energie ist aufgrund des Energieerhaltungssatzes nicht möglich. Die Bezeichnung „Energieerzeugung“ wird im Wirtschaftsleben aber dennoch verwendet, um die
Umwandlung einer bestimmten Energieform (zum Beispiel elektrischer Strom) aus einer anderen Form (zum Beispiel chemischer Energie in Form von Kohle) auszudrücken. Analog gibt
es im strengen physikalischen Sinne auch keinen „Energieverbrauch“, wirtschaftlich gemeint ist damit der Übergang von einer Energieform in eine andere.
Beispielsweise wird elektrische Energie „verbraucht“, um einen Ventilator zu betreiben. Die „verbrauchte“ elektrische Energie muss dann von uns bezahlt werden. Von
Energieeinsparung ist die Rede, wenn effizientere Prozesse gefunden werden, die weniger Primärenergie (Kohle, Gas, Öl) für denselben Zweck benötigen, oder anderweitig, zum
Beispiel durch Konsumverzicht, der Primärenergieeinsatz reduziert wird.
Die meisten Umwandlungen erfolgen nicht vollständig in eine einzige Energieform, sondern es wird ein Teil der Energie in Wärme gewandelt. In mechanischen Anwendungen wird die
Wärme meist durch Reibung erzeugt. Diese Wärme wird in der Regel nicht genutzt und als „Verlust“ bezeichnet. Das Verhältnis zwischen erfolgreich umgewandelter Energie und
eingesetzter Energie wird Wirkungsgrad genannt. Bei technischen Anwendungen wird häufig eine Reihe von Energieumwandlungen gekoppelt. In einem Kohlekraftwerk wird zunächst
die chemische Energie der Kohle durch Verbrennung in Wärme umgesetzt und auf Wasserdampf übertragen. Turbinen wandeln die Wärme des Dampfs in mechanische Energie um und treiben wiederum
Generatoren an, die die mechanische Energie in elektrische Energie umwandeln.
Während alle Energieformen unter gewissen Bedingungen vollständig in thermische Energie umgewandelt werden können, gilt das in umgekehrter Richtung nicht. Abhängig von der
Temperatur, bei der die Wärme zur Verfügung steht, lässt sich nur ein mehr oder weniger großer Anteil in mechanische Arbeit umwandeln, während der Rest an die Umgebung abgegeben wird.
-----------------------------------
Hinweis: Die Quellenangaben zu diesem Text sind am Ende dieser Internetseite zu finden.

Videos:
1) → Thermische Energie | alpha Lernen erklärt Physik [3:24]
2) → Energieformen - Überblick [4:09]
3) → Was ist Energie - Energieformen [5:29]
4) → Umwandlung der Energieformen [4:10]
Anmerkung: Die Links in diesem Ordner verweisen auf externe YouTube-Videos anderer YouTube-Kanäle. Gelegentlich werden Videos dort auch wieder entfernt. Entsprechende Hinweise zur Aktualisierung dieser Seite werden gerne per → Mail oder über das → Kontaktformular entgegengenommen. - Vielen Dank schon vorab für den Hinweis!
Aufgaben:
- Du willst einen Liter Wasser zum Kochen bringen. Wie kannst du vorgehen?
a) Nenne drei verschiedenen Möglichkeiten.
b) Was ist bei deinen verschiedenen Möglichkeiten jeweils die Energiequelle? - Nenne fünf Energieformen und jeweils mindestens ein Beispiel dazu.
- Die Einheit der Energie wurde nach einem englischen Physiker benannt. Wer war das, wann lebte er und wo wurde er geboren?
- Kann Energie „verloren“ gehen? Beschreibe deine Überlegung an einem Beispiel und erläutere deine Antwort genau.
- Was ist der Unterschied zwischen Wärme und Temperatur?
- Beschreibe den Unterschied zwischen Wärme und Temperatur anhand der folgenden Überlegung:
Erstens: Du erhitzt einen Liter Wasser mit einem Tauchsieder von 20°C auf 30°C. (Anschließend hat das Wasser die Temperatur von 30°C.)
Zweitens: Du erhitzt zwei Liter Wasser mit dem gleichen Tauchsieder ebenfalls von 20°C auf 30°C. (Anschließend hat das Wasser ebenfalls eine Temperatur von 30°C.)
Frage: Haben wir dafür aber auch die gleiche Energie benötigt? Welcher entscheidende Unterschied ist bei dem Versuch festzustellen? - Zwei Liter Wasser werden vermischt. Der eine Liter Wasser hatte zunächst eine Temperatur von 20°C, der zweite Liter Wasser dagegen eine Temperatur von 50°C. Was kannst du über die Temperatur und die Energie bei diesem Versuch sagen?

Infos zum Thema (planet-schule.de):

Planet Schule
Planet Schule bietet Schulfernsehsendungen zum Ansehen und Herunterladen so wie weitere Lernangebote für Lehrer, Schüler und natürlich alle Bildungsinteressierten.
Produktlinks (amazon.de)
Alle von mir erstellten Materialien stehen für Bildungszwecke frei zur
Verfügung, dürfen allerdings nicht von jemand anderem kommerziell vertrieben werden.
Hinweis: Es werden keine Bücher oder sonstige, hier benannte Materialien im
Unterricht verwendet oder benötigt.

Quellenangaben zu den Inhalten auf dieser Seite
Infotext ([01] Wärmelehre - Wärmelehre)
 Dieser Text basiert auf den Artikeln Thermodynamik und Aggregatzustand aus der freien Enzyklopädie Wikipedia und steht unter der Lizenz Creative Commons CC-BY-SA 3.0 Unported (Kurzfassung). Der
Text wurde von Andreas Rueff überarbeitet und auf der Grundlage didaktischer Überlegungen angepasst und gekürzt. In der Wikipedia ist
eine Liste der Autoren verfügbar.
Dieser Text basiert auf den Artikeln Thermodynamik und Aggregatzustand aus der freien Enzyklopädie Wikipedia und steht unter der Lizenz Creative Commons CC-BY-SA 3.0 Unported (Kurzfassung). Der
Text wurde von Andreas Rueff überarbeitet und auf der Grundlage didaktischer Überlegungen angepasst und gekürzt. In der Wikipedia ist
eine Liste der Autoren verfügbar.
Bild von Pexels auf Pixabay
Bild von Monika auf
Pixabay
Bild von Pexels auf Pixabay
Bild von Анастасия Белоусова
auf Pixabay
Infotext ([02] Wärmelehre - Temperatur messen
 Dieser Text basiert auf den Artikeln Thermometer und Thermorezeption aus der freien Enzyklopädie Wikipedia und steht unter der Lizenz Creative Commons CC-BY-SA 3.0 Unported (Kurzfassung). Der
Text wurde von Andreas Rueff überarbeitet und auf der Grundlage didaktischer Überlegungen angepasst und gekürzt. In der Wikipedia ist
eine Liste der Autoren verfügbar. (Abb.: Pixabay, bearbeitet von A. Rueff)
Dieser Text basiert auf den Artikeln Thermometer und Thermorezeption aus der freien Enzyklopädie Wikipedia und steht unter der Lizenz Creative Commons CC-BY-SA 3.0 Unported (Kurzfassung). Der
Text wurde von Andreas Rueff überarbeitet und auf der Grundlage didaktischer Überlegungen angepasst und gekürzt. In der Wikipedia ist
eine Liste der Autoren verfügbar. (Abb.: Pixabay, bearbeitet von A. Rueff)
 Dieser Text basiert auf dem Artikel Teilchenmodell aus der freien
Enzyklopädie Wikipedia und steht unter der Lizenz Creative Commons CC-BY-SA 3.0
Unported (Kurzfassung). Der Text wurde von Andreas Rueff
überarbeitet und auf der Grundlage didaktischer Überlegungen angepasst und gekürzt. In der Wikipedia ist eine Liste der Autoren verfügbar.
Dieser Text basiert auf dem Artikel Teilchenmodell aus der freien
Enzyklopädie Wikipedia und steht unter der Lizenz Creative Commons CC-BY-SA 3.0
Unported (Kurzfassung). Der Text wurde von Andreas Rueff
überarbeitet und auf der Grundlage didaktischer Überlegungen angepasst und gekürzt. In der Wikipedia ist eine Liste der Autoren verfügbar.
 Dieser Text basiert auf den Artikeln Benjamin Franklin und Ölfleckversuch aus der freien Enzyklopädie Wikipedia und steht unter der Lizenz Creative Commons CC-BY-SA 3.0 Unported (Kurzfassung). Der
Text wurde von Andreas Rueff überarbeitet und auf der Grundlage didaktischer Überlegungen angepasst und gekürzt. In der Wikipedia ist
eine Liste der Autoren verfügbar.
Dieser Text basiert auf den Artikeln Benjamin Franklin und Ölfleckversuch aus der freien Enzyklopädie Wikipedia und steht unter der Lizenz Creative Commons CC-BY-SA 3.0 Unported (Kurzfassung). Der
Text wurde von Andreas Rueff überarbeitet und auf der Grundlage didaktischer Überlegungen angepasst und gekürzt. In der Wikipedia ist
eine Liste der Autoren verfügbar.
 Dieser Text basiert auf den Artikeln Wärmeausdehnung und Flüssigkeitsthermometer aus der freien Enzyklopädie Wikipedia und steht unter der
Lizenz Creative Commons CC-BY-SA 3.0 Unported (Kurzfassung). Der Text wurde von Andreas Rueff überarbeitet und auf der
Grundlage didaktischer Überlegungen angepasst und gekürzt. In der Wikipedia ist eine Liste der Autoren verfügbar.
Dieser Text basiert auf den Artikeln Wärmeausdehnung und Flüssigkeitsthermometer aus der freien Enzyklopädie Wikipedia und steht unter der
Lizenz Creative Commons CC-BY-SA 3.0 Unported (Kurzfassung). Der Text wurde von Andreas Rueff überarbeitet und auf der
Grundlage didaktischer Überlegungen angepasst und gekürzt. In der Wikipedia ist eine Liste der Autoren verfügbar.
 Dieser Text basiert auf den Artikeln Anders Celsius und Grad Fahrenheit aus der freien Enzyklopädie Wikipedia und steht unter der Lizenz Creative Commons CC-BY-SA 3.0 Unported (Kurzfassung). Der
Text wurde von Andreas Rueff überarbeitet und auf der Grundlage didaktischer Überlegungen angepasst und gekürzt. In der Wikipedia ist
eine Liste der Autoren verfügbar.
Dieser Text basiert auf den Artikeln Anders Celsius und Grad Fahrenheit aus der freien Enzyklopädie Wikipedia und steht unter der Lizenz Creative Commons CC-BY-SA 3.0 Unported (Kurzfassung). Der
Text wurde von Andreas Rueff überarbeitet und auf der Grundlage didaktischer Überlegungen angepasst und gekürzt. In der Wikipedia ist
eine Liste der Autoren verfügbar.
 Dieser Text basiert auf den Artikeln Robert Brown (Botaniker,
1773) und Brownsche Bewegung aus der freien Enzyklopädie Wikipedia und steht unter
der Lizenz Creative Commons CC-BY-SA 3.0 Unported (Kurzfassung). Der Text wurde von Andreas Rueff überarbeitet und auf der
Grundlage didaktischer Überlegungen angepasst und gekürzt. In der Wikipedia ist eine Liste der Autoren verfügbar.
Dieser Text basiert auf den Artikeln Robert Brown (Botaniker,
1773) und Brownsche Bewegung aus der freien Enzyklopädie Wikipedia und steht unter
der Lizenz Creative Commons CC-BY-SA 3.0 Unported (Kurzfassung). Der Text wurde von Andreas Rueff überarbeitet und auf der
Grundlage didaktischer Überlegungen angepasst und gekürzt. In der Wikipedia ist eine Liste der Autoren verfügbar.
 Dieser Text basiert auf den Artikeln Energie und James Prescott Joule aus der freien Enzyklopädie Wikipedia und steht unter der Lizenz Creative Commons CC-BY-SA 3.0 Unported (Kurzfassung). Der
Text wurde von Andreas Rueff überarbeitet und auf der Grundlage didaktischer Überlegungen angepasst und gekürzt. In der Wikipedia ist
eine Liste der Autoren verfügbar.
Dieser Text basiert auf den Artikeln Energie und James Prescott Joule aus der freien Enzyklopädie Wikipedia und steht unter der Lizenz Creative Commons CC-BY-SA 3.0 Unported (Kurzfassung). Der
Text wurde von Andreas Rueff überarbeitet und auf der Grundlage didaktischer Überlegungen angepasst und gekürzt. In der Wikipedia ist
eine Liste der Autoren verfügbar.
Die Abbildungen wurden von Pixabay entnommen.
Using PhET Simulations in Teaching
-
Simulation by PhET Interactive Simulations, University of Colorado Boulder, licensed under CC-BY-4.0 (https://phet.colorado.edu).
Aus dieser Seite sind Online-Übungen eingebunden. Diese sind bei www.learningapps.org erstellt worden, es kann sich auch teilweise um Apps von externen Erstellern handeln.
Hintergrundbild: Eigenes Bild (Rueff)





































